A produção in vitro de embriões (PIVE) é uma biotécnica reprodutiva considerada uma ferramenta valiosa para a melhoria da eficiência reprodutiva e também da genética do rebanho.
Ela permite recolher oócitos de uma fêmea (doadora), manipulá-la em laboratório para maturarem, serem fecundados e desenvolverem em embriões para então transferi-los para fêmeas (receptoras) com a finalidade de completarem o período de gestação.
Nesse artigo iremos abordar o passo a passo das etapas necessárias para a produção in vitro de embriões bovinos, incluindo desde a coleta dos oócitos até a criopreservação ou transferência para o animal receptor e também trataremos sobre as principais vantagens da utilização dessa biotecnologia reprodutiva.
Sem tempo para ler agora? Baixe este artigo em PDF!
Produção de embriões in vitro: da aspiração folicular à transferência
Para que seja possível realizar a produção de embriões in vitro, uma série de passos complexos e especializados são envolvidos, entretanto, podemos resumir o processo da seguinte maneira:
- Doadora 🡪 Aspiração folicular (oócitos imaturos) 🡪 Maturação (metáfise II) 🡪 Fecundação 🡪 Desnudação do zigoto 🡪 Cultivo in vitro por 7 dias (desenvolvimento – primeiras clivagens: mórula – blastócito) 🡪 Transferência para a receptora previamente sincronizada ou congelamento.
Quando se trata desse assunto, é importante lembrar que todo o processo que ocorre em laboratório tem a intenção de simular o que de fato acontece fisiologicamente no animal. Por isso, é essencial entendermos o ciclo estral da vaca e também sobre as ondas de crescimento folicular:
- Onda de crescimento folicular 🡪 Aumento do Hormônio Folículo Estimulante (FSH) 🡪 Recrutamento folicular 🡪 Seleção 🡪 Dominância 🡪 Folículo Dominante (FD) 🡪 Progesterona (P4) baixa nesse momento (ausência de Corpo Lúteo (CL) ativo) e aumento do Estradiol (E2) levando ao pico do Hormônio Luteinizante (LH) 🡪 Ovulação do oócito em metáfase II (maduro para ser fecundado).
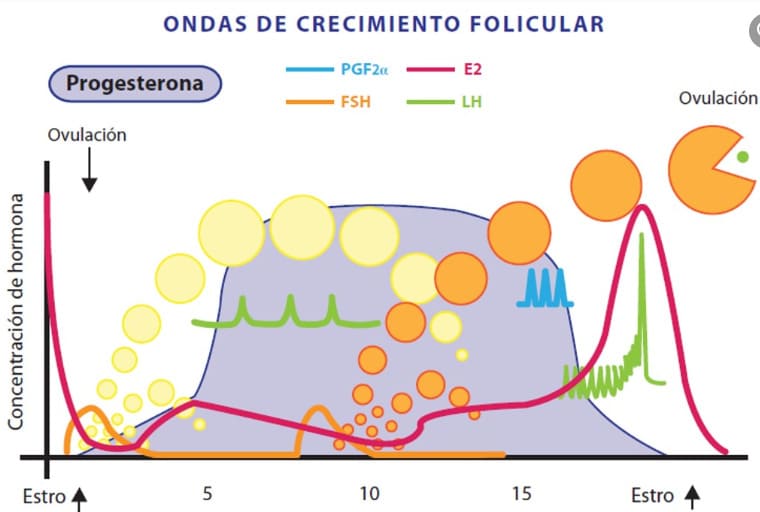
Esquema do ciclo estral das fêmeas bovinas, evidenciando as ondas foliculares e comportamento e ação dos hormônios até a ovulação. Fonte: Genética y Biotecnologías Reproductivas
Sabendo então o oócito maduro (em metáfise II), ou seja, pronto para ser fecundado é o oócito ovulado durante um ciclo estral natural da vaca e que quando realizamos a produção in vitro de embriões estamos coletando o oócito antes dessa fase, ou seja, aspiramos os oócitos ainda em desenvolvimento teremos ele imaturos para a fecundação, tornando necessário então uma fase onde esses oócitos serão maturados e estarão prontos para receber a fecundação.
Quais as etapas da produção in vitro de embriões?
Quanto às etapas que constituem a PIVE, podemos citar:
- Colheita de oócitos;
- Maturação in vitro (MIV);
- Fecundação in vitro (FIV);
- Cultivo in vitro (CIV);
- Criopreservação ou transferência de embriões.
Colheita de oócitos
Essa etapa consiste em recuperar gametas femininos para a manipulação in vitro. A punção folicular guiada por ultrassom (Ovum pick up – OPU) é a forma mais utilizada em fazendas comerciais e para que seja realizada alguns pontos são de grande relevância:
- É necessário que seja realizada anestesia epidural das vacas que passarão pela punção folicular e também a higienização do reto e da vulva.
- Mão introduzida no reto 🡪 Traciona o ovário o mais próximo da cérvix 🡪 Com o auxílio da probe de ultrassom é possível observar os folículos a serem aspirados.
- Acoplado ao madril, tem-se a agulha que fará a punção. Essa agulha estará acoplada a um sistema de bomba a vácuo que permite que o material puncionado caia dentro de um tubo.
- Não é necessário o uso de hormônios para a recuperação dos oócitos, mas para ter mais sucesso com a aspiração folicular pode-se aplicar um protocolo de superovulação nas vacas, sendo assim opcional.
- Aspira-se cerca de 20 oócitos de cada vaca, tendo 8 oócitos viáveis em média.
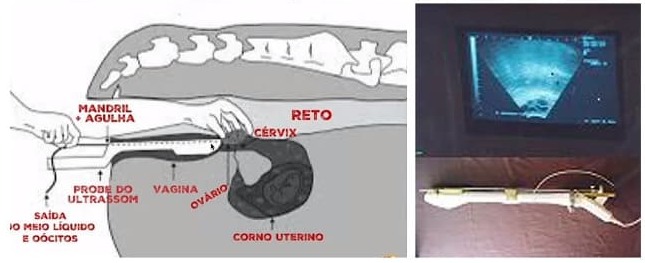
Imagem ilustrando a aspiração folicular guiada por ultrassom. Fonte: Renata Lançoni
Maturação in vitro (MIV)
Sabemos que os oócitos coletados ainda são imaturos, o que confere a necessidade de passarem por uma seleção em microscópio a fim de eleger os oócitos viáveis, para que, por fim eles sejam maturados (etapa de maturação in vitro) e entrem em metáfase II.
Essa etapa de seleção dos oócitos de boa qualidade é essencial para a PIVE e nela haverá a classificação dos mesmos a partir da avaliação do Complexo Cumulus-Oócito (COC), onde podem receber as seguintes classificações:
- Oócitos grau I: 3 ou mais camadas de células do cumulus, citoplasma homogêneo.
- Oócitos grau II: 2 ou mais camadas de células do cumulus, citoplasma homogêneo.
- Oócitos grau III: camada incompleta de células do cumulus, citoplasma homogêneo ou heterogêneo.
- Oócitos grau IV: degenerado, desnudo (sem células do cumulus)🡪 se utilizar esse oócito estará prejudicando a maturação e posteriormente o desenvolvimento embrionário.
Nessa seleção, a prioridade sempre será deter de oócitos nas classificações grau I e grau II.
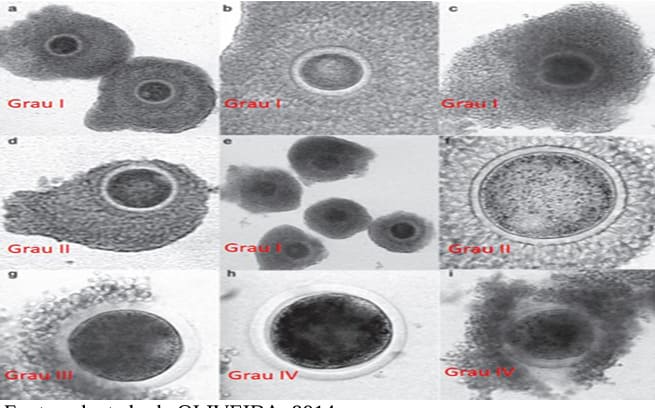
Visualização morfológica de oócitos em diferentes graus. Fonte: Adaptado de Oliveira, 2014.
Meio de maturação
Os oócitos selecionados seguem então para a etapa de maturação, onde é necessário ter um meio de maturação comercial, que recebe adição de antibióticos para evitar contaminações, soro fetal bovino/albumina e hormônios (LH e FSH).
A maturação tem duração de 18 a 24 horas em atmosfera controlada, contendo 5% de CO² em ar e umidade saturada de 38,5°C. Para que ocorra a passagem dos oócitos imaturos para oócitos maduros, alterações no núcleo e citoplasma acontecem, pois teremos a passagem do estágio de prófase I – 4n para a metáfise II – 2n.
É importante ressaltar que não adianta ter só a maturação nuclear e não ocorrer a maturação citoplasmática, ambas devem acontecer em conjunto. Após essas 18-24 horas o Cumulus é expandido, o que mostra que o oócito foi maturado.
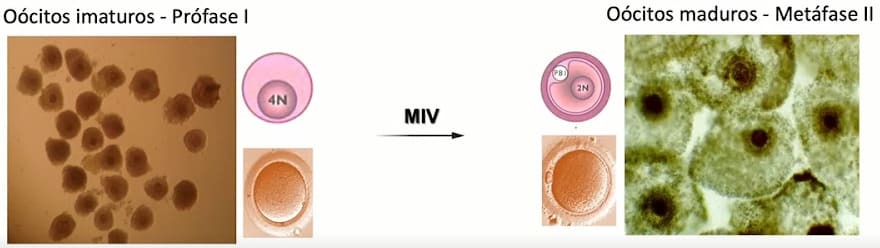
Esquema demonstrando a transformação de oócitos imaturos para oócitos maduros. Fonte: Renata Lançoni
Fecundação in vitro (FIV)
Essa etapa de fecundação consiste em colocar os espermatozoides junto com o oócito. Para isso, os oócitos são lavados em meio FIV e os espermatozoides precisam ser previamente preparados.
- Para fecundação, normalmente utiliza-se o sêmen criopreservado/convencional, mas o sêmen sexado e o sêmen a fresco também podem ser utilizados.
- Na escolha do sêmen, a utilização do sêmen sexado (capaz de produzir descendentes machos ou fêmeas, ou seja, permite a seleção do sexo na concepção) permite reduzir o tempo para atingir certos objetivos.
- Na maioria dos laboratórios, utiliza-se sêmen congelado/criopreservado para o processo de fecundação in vitro em bovinos. No entanto, após o descongelamento, é necessário selecionar os espermatozoides vivos e capazes de fecundar. Esta seleção é realizada, na maioria das vezes, pela separação em gradiente de Percoll, embora outros sistemas possam ser utilizados como o “swim-up” ou o lavado espermático.
Sobre esse preparo dos espermatozoides até a deposição na gota de FIV:
- Descongelar o sêmen (37°C/30seg).
- Submeter o volume da palheta (0,25 ml) ao gradiente de Percoll (sêmen|diluidor + espermatozoides).
- Gradiente de Percoll 45% e Percoll 90%.
- Centrifugação.
- Separação dos espermatozoides viáveis dos não viáveis (mortos.)
- Parte superior = diluidor | Percoll 45% = espermatozoides inviáveis (sem motilidade) | Pelets = espermatozoides viáveis (com motilidade).
- Lavagem + centrifugação + meio de fecundação.
- Ajustar o volume e depositar espermatozoides na gota de FIV em oócitos – Normalmente utiliza 1 milhão de espermatozoide por ml, podendo chegar a até 2 milhões. Quando aumenta muito o número de espermatozoides por ml, aumentamos também a chance de ocorrer polispermia, ou seja, mais de um espermatozoide penetrando no oócito, resultando em um zigoto poliploide e normalmente inviável.
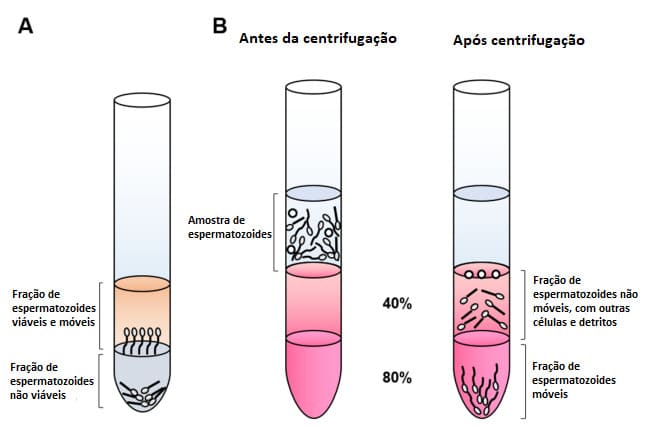
A- Diagrama da base do Swim Up: Os espermatozoides móveis são separados “nadando” até a superfície do meio de cultura.
B- Esquema da base do Gradiente de Densidade – Percoll: Os espermatozoides móveis são separados do resto das células por uma diferença de densidade. Após centrifugação em gradientes contínuos e descontínuos, a fração móvel dos espermatozoides fica localizada na parte inferior.
Fonte: Adaptado de In Vitro Buenos Aires
Meio de fecundação
O meio de fecundação que é utilizado nessa fase contém agentes capacitantes, albumina e antibiótico.
Essa fase de fecundação tem duração de 18 horas também em atmosfera controlada contendo 5% de CO² em ar e umidade saturada a 38,5°C. É nesse período que ocorrerá a capacitação espermática, ou seja, espermatozoides passando por severas mudanças bioquímicas e fisiológicas para se tornarem aptos à fertilização e consigam ultrapassar a barreira de células do Cumulus.
De fato, a fecundação ocorre quando o espermatozoide atinge a zona pelúcida, digere e toca no citoplasma. É nesse momento que se tem o bloqueio da polispermia, a partir do endurecimento da zona pelúcida.
Cultivo in vitro (CIV)
Após fecundados, os presumíveis embriões estão prontos para serem cultivados e nessa fase alguns eventos devem acontecer para que por fim tenhamos embriões prontos para serem transferidos ou criopreservados:
- Retirada do excesso das células do Cumulus dos embriões, o que chamamos de desnuda.
- Lavagem e colocação em meio de cultivo SOF – criado com base na constituição de fluido do oviduto de bovinos (com ou sem co-cultivo das células do Cumulus).
- Em cada gota (0,5 ml), colocar em média 100 microlitros da solução de cultivo.
- Alta tensão de oxigênio (20% de oxigênio e 5% de CO2) X baixa tensão de oxigênio (5% de oxigênio – isso é benéfico para os embriões, pois reduz as espécies reativas de oxigênio, produzindo embriões de melhor qualidade, mais claros e com menor acúmulo de lipídios), entretanto, os embriões de baixa tensão de oxigênio são sensíveis a variações de oxigênio, então se abre muito a estufa para manipular, eles sofrem bastante.
- Alguns laboratórios realizam o que chamamos de Feeding e avaliação da clivagem no dia 3 de desenvolvimento. Com isso pode renovar o meio, adicionando meio fresco para dar mais componentes para o embrião – entrando devemos seguir a premissa de menor manipulação nesse embrião em desenvolvimento e sermos críticos quanto a esse método.
- Cultivo até o 7º dia de desenvolvimento 🡪 Blastocisto.
- Blastocisto = momento em que se faz a transferência para as receptoras ou quando faz o congelamento.

Esquema demonstrando que o D0 corresponde ao dia da FIV. No D3 temos a clivagem e no D7 o estágio de blastocisto. Fonte: Renata Lançoni
Período de desenvolvimento inicial → divisão celular → ativação do genoma embrionário (aproximadamente 8 células) → compactação (mórula → mórula compacta) → formação da blastocele (mórula → blastocisto).
No D7 espera-se encontrar o embrião em estádio de blastocisto, com blastocele (cavidade) e massa celular interna. Nesse dia o embrião deve ser transferido para receptora ou criopreservado.
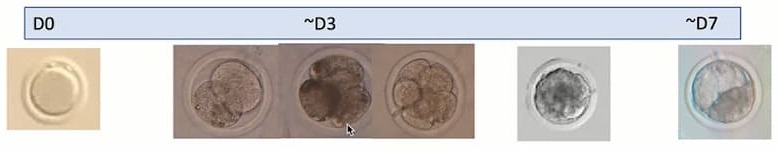
Imagem ilustrando a morfologia do embrião nos diferentes dias após a FIV. Fonte: Renata Lançoni
Criopreservação ou transferência do embrião
Após cultivados, os embriões em forma de blastocisto são envasados em palhetas e diretamente transferidos a fresco para as receptoras devidamente sincronizadas, ou podem também ser criopreservados (mantidos em nitrogênio líquido) antes de serem transferidos.
Embriões in vitro x in vivo (2019):
- In vivo: 60% do total de embriões produzidos in vivo transferidos foram de embriões criopreservados (240.000 de 400.000 embriões).
- In vitro: 45% do total de embriões produzidos in vitro transferidos foram de embriões criopreservados (450.000 de 1.000.000 embriões).
O objetivo da criopreservação de embriões é manter a viabilidade embrionária por longo período em estado de letargia que seja reversível pós-descongelação.
Vantagens da criopreservação
- Aproveitamento dos embriões excedentes.
- Aproveitamento de receptoras excedentes.
- Facilidade de comércio.
- Escolha da data de parto.
- Banco de germoplasma.
Quais as vantagens da produção in vitro de embriões?
- Aceleração da disseminação de material genético superior: A PIVE permite que as fazendas reproduzam geneticamente animais superiores, por exemplo em termos de produção de leite, eficiência alimentar e resistência a doenças. Ou seja, é possível ter melhor aproveitamento do potencial genético das fêmeas e a redução do intervalo de gerações (idade média dos pais quando nascem os filhos), o que é benéfico quando se pensa em ganho genético anual.
- Uso eficiente de animais geneticamente superiores: Animais geneticamente superiores podem ser selecionados como doadores, o que permite termos um número significativo de descendentes advindos desses animais, o que otimiza o uso eficiente de animais de alto valor genético.
- Aumento na taxa de multiplicação: Possibilidade de produção de múltiplos embriões a partir de um único animal doador, o que amplia a taxa de multiplicação genética.
- Aprimoramento da eficiência reprodutiva: A PIVE é uma ferramenta útil em casos de dificuldades reprodutivas em animais ou quando se tem o desejo de maximizar o uso de fêmeas com alto valor genético, mas que podem ter limitações reprodutivas naturais.
- Melhora na produção de leite e eficiência alimentar: Ao selecionar animais com características genéticas associadas a uma produção de leite mais eficiente e uma melhor eficiência alimentar, a PIVE contribui para aprimorar o desempenho produtivo do rebanho.
Considerações finais
Em resumo, a produção in vitro de embriões em vacas leiteiras é uma tecnologia que desempenha um papel crucial na otimização do potencial genético dos rebanhos, permitindo a reprodução seletiva de características desejáveis e a produção eficiente de descendentes de animais geneticamente superiores.
Isso, por sua vez, impacta positivamente na produtividade, qualidade e sustentabilidade da produção leiteira.
Tecnologia reprodutiva para acelerar o progresso genético e produtivo
A produção in vitro de embriões é uma ferramenta poderosa para melhorar a genética, aumentar a produtividade e encurtar o intervalo entre gerações no rebanho.
Na Pós-graduação em Pecuária Leiteira do Rehagro, você aprende a integrar biotecnologia, manejo reprodutivo e gestão para obter resultados de alto impacto na fazenda.












Parabéns. Excelente artigo. Muito bem explicado.
Oi Oderman,
Ficamos felizes que você tenha gostado do nosso conteúdo! Sua interação aqui conosco é muito importante para nós.
Já conferiu nosso catálogo de cursos? Com certeza temos um curso que te atenderá, contribuindo muito para seu desenvolvimento na pecuária leiteira. Esperamos por você!!